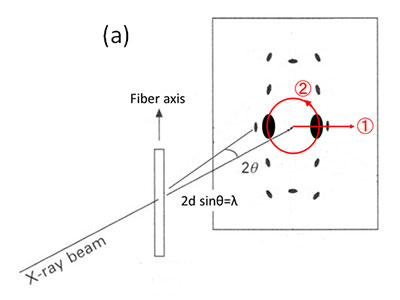
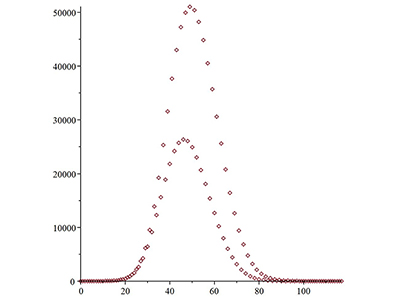
おもしろ科学実験室(工学のふしぎな世界)
手のひらのホワイトクリスマス
~おうちでできる結晶シリーズ~
京都工芸繊維大学 高度技術支援センター
小川奈津美
少しだけお勉強
食塩(溶質)を水(溶媒)に溶かすとき、水(溶媒)の量と温度が一定であれば、食塩(溶質)が溶ける量はそれぞれ決まっています。溶媒に溶質がどのくらい溶けるかを表した数値は「溶解度」と呼ばれます。溶質を溶媒に溶かした液体は「溶液」と呼ばれ、溶質をそれ以上溶けなくなるまで溶かした溶液は「飽和溶液」と言います。
一般的に、溶解度は溶媒の温度が高いほど大きくなり、温度が低いと小さくなります。例えば、熱いお湯に砂糖はたくさん溶けますが、冷たい水にはあまり溶けません。砂糖の熱い飽和水溶液をゆっくり冷やしていくと、温度が下がるにつれて、砂糖が溶けきれなくなって、水の中から出てきます。出てきた砂糖は「結晶」となります(氷砂糖ですね)。高温と低温で溶解度の差が大きいほど、出てくる結晶の量は多くなります。
一方、食塩の溶解度は温度を上げてもあまり差がないため、食塩の熱い飽和水溶液を冷やしても、砂糖ほどには結晶が出てきません。
それでは、飽和食塩水から食塩の結晶を取り出すには、どうすれば良いでしょうか?もちろん、色々な方法がありますが、実験を行いながら、今回はどういう仕組みで取り出しているのか考えていきましょう。
準備する物

- 水 100mL
- 食塩 40g程度
- 無水エタノール 10 mL
- ボトル(内容量130mL程度) 1個
- ボトル内の飾り 任意
- スポイト 2本
- 飽和食塩水用ふた付き容器 1個
実験で使うボトルは、エタノール(アルコール)に強い素材を選んでください。
例:ガラス、PP(ポリプロピレン)、PE(ポリエチレン)、硬質PVC(ポリ塩化ビニル)
プラスチック製品は、材質によってはエタノールに溶けたり変形することがあります。
製品の注意事項やタグをよく確認してから、実験を行うようにしてください。
事前準備 ボトルの飾り付け
「モール 工作」などのキーワードで検索すると、作り方や作例が出てきます。

ビニールタイと飾りの端を結んで、中で開いて固定

事前準備 飽和食塩水の調製

※飽和食塩水は食塩が溶けるのに時間がかかります。実験の前日に調製しておくことをお勧めします。
ふた付きの容器に水(100mL)を入れます。
はかりで食塩(40g)をはかりとります。
はかりとった食塩を大さじ1杯程度取り、容器の水の中に入れ、よくかき混ぜて溶かします。これを何回か繰り返し、はかりとった食塩をすべて容器の中に入れたら、よくかき混ぜます。
容器の底に食塩が溶け残っていることを確認します。
一晩程度室温で置いて、完成です。
※食塩が溶けきった場合は、小さじ1杯程度食塩を追加してください。
実験手順
手順1
ボトルに飽和食塩水の上澄み(約100mL)を入れます。

手順2
エタノール(10mL)をスポイトを使って飽和食塩水の上に静かに注ぎます。

手順3
容器の上部を持って静かに揺らし、エタノールと飽和食塩水の境目を揺らして一部を混ぜます。
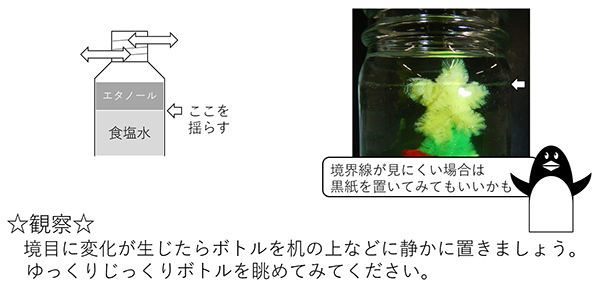
手順4
ボトル内の変化がなくなったら、再度容器を揺らします。

手順5
最後に境目が分からなくなるまで軽く揺らします。
液面が完全に変化しなくなったら、様子を観察してみましょう。
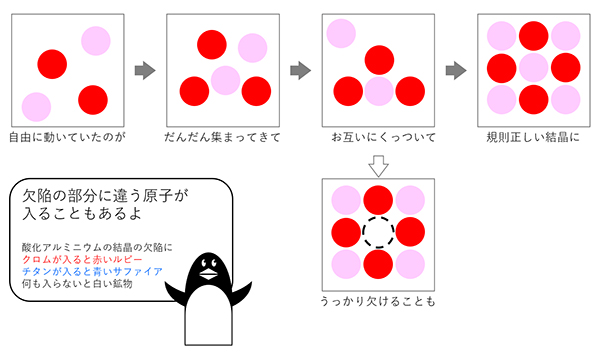
結晶の成長イメージ
| 掲載大学 学部 |
京都工芸繊維大学 工芸科学部 | 京都工芸繊維大学 工芸科学部のページへ>> |
- ※このページに含まれる情報は、掲載時点のものになります。