おもしろ科学実験室(工学のふしぎな世界)
軽くて機能を持つ材料
~導電性高分子でエレクトロクロミズムと二次電池を知ろう~
香川大学 創造工学部
はじめに
高分子は、“(価格の)高い分子”ではなく、分子量の大きな有機分子(炭素、水素、酸素などからできている分子量が10000以上のもの)のことです。皆さんの身の回りにあるプラスチックが代表例です。分子量の小さい分子(低分子)とは異なり、プラスチックなどの高分子は沸騰することはなく、加熱や加圧で容易に変形、加工できる特徴があります。また、プラスチックでもわかるように多くの高分子は“電気が流れない”ため、電子機器の絶縁体などに利用されていました。しかし、1970年代に白川英樹博士らにより開発された導電性高分子は、名前の通り「電気が流れる」高分子であり、容易に加工でき軽量の高分子は様々な電池、センサなどの材料に利用され、電子機器の小型・軽量化、高機能化などに大きく貢献しています。2000年には導電性高分子の発見と開発に貢献した白川先生をはじめとする3名の研究者にノーベル化学賞が授与されています。
導電性高分子は電気が流れるだけでなく、電子状態が変わると、電気的性質が大きく変わるだけでなく、色変化や発光することも報告されています。今回は、この導電性高分子をアニリンの酸化重合で合成し、エレクトロクロミズムを見ること、さらには充電・放電を繰り返すことが可能な二次電池となることを見ていきます。
原理
エレクトロクロミズム (Electrochromism) とは、電圧を印加することにより、分子が酸化・還元反応を起こし、異なる状態(ラジカル状態など)なることで色が変化する現象です。ボーイング787の電子カーテンなどはエレクトロクロミズムの応用例として有名です。
1回の放電後使用できなくなる一次電池とは異なり、二次電池は充電が可能な電池のことです。様々なモバイル電子機器には欠かせないリチウムイオン電池も二次電池であり、軽量化、低価格化、高効率化が望まれています。
電解重合とは、電気が流れる電解質溶液(NaClなど水などに溶けることで電離したイオンが存在する溶液)中で、電極の電圧を変化させ、分子が電極上で酸化・還元反応を起こし、分子同士が連続して結合する(プラスチック(高分子)ができる)方法のことです。ここで用いるアニリンは酸化することで重合していきます(図1)。
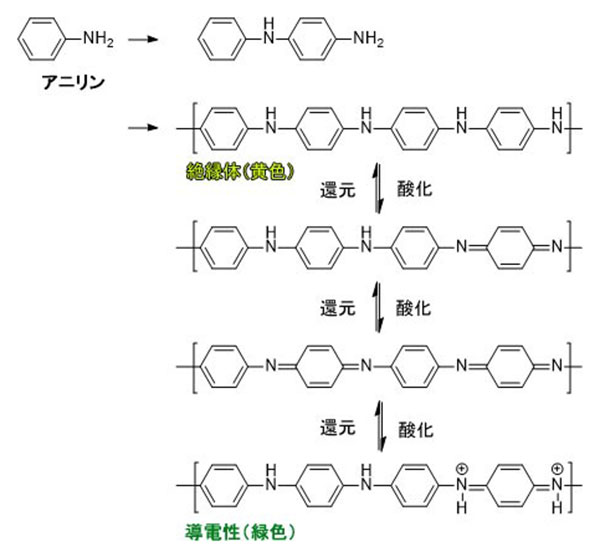 図1 アニリンの酸化重合の反応式。酸化が進むことで、導電性を発現します。
図1 アニリンの酸化重合の反応式。酸化が進むことで、導電性を発現します。準備するもの
- 溶液A:アニリン 0.5 mol/L + 過塩素酸 2.0 mol/Lの混合水溶液
- 溶液B:0.1 mol/Lの過塩素酸リチウム水溶液
- 50 mlまたは100 mlのビーカー2つ
- ワニ口クリップ2本(シリコン栓または割り箸に落ちないように固定したもの)
- ステンレス板2枚 亜鉛板 1枚
- 乾電池と乾電池ホルダー 1組
- 圧電ブザー(1.5 Vで駆動するもの) 1つ
- デジタルマルチメーター(テスター.電圧、電流を測る装置) 1つ
- キムタオル2枚
- 使用する薬品は簡単に入手できないため、化学系の教員の下で実験を行ってください。
- 溶液Aは強酸です。手についた場合は、速やかに石鹸を使って、手を洗ってください。服に付着すると穴が開く場合もあります。実験中は手袋、ゴーグル、白衣(または安全服)を着用してください。
- 後片付けにおいて、使用した溶液はいずれも水溶液ですが、アニリンが含まれる溶液Aは実験廃液として適切に廃棄してください。(ただし、比較的繰り返し利用できるので、保管して改めて利用することも可能です。)
- ステンレス板についたポリアニリンは紙である程度簡単にふき取れます。どうしても取れない場合は、有機溶媒で洗い流すなどを行います。
実験
- 固定されたワニ口クリップにそれぞれステンレス板(電極)を挟み、電極を溶液Aにつけ、それぞれの電極を付けたワニ口クリップを乾電池の+極と-極につなぎます。
(*この時、ワニ口クリップが溶液に付かないようにすること。また、ステンレス電極同士も接触させないようにすること。) - +極のステンレス板は、時間とともに溶液に浸かっている部分が深緑色~黒色になり、膜のようなものがついていることが確認できます(図2)。 これはアニリンが重合し、ポリアニリンという導電性高分子が生成されているためです。また、-極側はガスが発生していることがわかります。
 図2 ポリアニリンの電界重合。電池の+極につながっているステンレス板には、緑色の膜のような物質が付着している。これがポリアニリン。(溶液は少しアニリンが酸化したため、褐色ですが、新しいアニリンであれば無色透明です。またポリアニリンは時間をかけると全体につきます。部分的についているだけでも、充電・放電はできます。)
図2 ポリアニリンの電界重合。電池の+極につながっているステンレス板には、緑色の膜のような物質が付着している。これがポリアニリン。(溶液は少しアニリンが酸化したため、褐色ですが、新しいアニリンであれば無色透明です。またポリアニリンは時間をかけると全体につきます。部分的についているだけでも、充電・放電はできます。)- 次に、一旦電池を外し、-極のステンレス板を亜鉛板に交換し、両方の電極を溶液Bにつけ、テスターで電極の電圧を測ります。すると、起電力が約+1.5 V示すことが確認できます(図3)。
 図3 導電性ポリアニリンの起電力。
図3 導電性ポリアニリンの起電力。- この状態で圧電ブザーをつなぎます(図4左)。するとブザーが振動とともになり始めます。乾電池でつないだ時と同様の状態であり、一種の電池の状態になっていることがわかると思います。ポリアニリンの状況にもよりますが、約1分程度振動が続きます。なり終わった際、ポリアニリンの色は黄緑色~黄色に変化します(図4右)。これは絶縁体の状態になっていることを示しています。圧電ブザーが止まったら、テスターで起電力を測ると先ほどよりも低くなっていることが確認できます。
 図4 圧電ブザーをつないだ実験。(左)実験の様子。(右)電極上に生成されたポリアニリンの色変化。圧電ブザーをつなげることで、電子が移動、放電されるため絶縁体に変化する。
図4 圧電ブザーをつないだ実験。(左)実験の様子。(右)電極上に生成されたポリアニリンの色変化。圧電ブザーをつなげることで、電子が移動、放電されるため絶縁体に変化する。- 再度、乾電池につなげるとポリアニリンは再び深緑色~黒色に変化します。充電が行われ、再び導電性のポリアニリンの状態に戻ったことを示します。再び圧電ブザーをつなげると、先ほど同様にブザーが鳴ります。
参考動画
香川大学創造工学部材料物質科学コース(旧先端マテリアル科学コース)では、上記内容の簡単な実験動画をYouTubeで公開しています。参考にしてください。
| 掲載大学 学部 |
香川大学 創造工学部 | 香川大学 創造工学部のページへ>> |