おもしろ科学実験室(工学のふしぎな世界)
化学反応の見える化!
山口大学 工学部
はじめに
化学反応は分子や原子が結合や切断、あるいは電子を放出したり受け取ったりすることで物質の構造が変化することを示します。しかし分子や原子は非常に小さいため肉眼では見えません。この化学反応が起こるとその化合物の集まったものは色が変わることで反応が進んでいることが分かります。
例えば酸塩基滴定で使用する指示薬のフェノールフタレインはpHの大きさで化学構造が変化し無色-淡赤-赤で反応が進行していることが分かります。

図1 フェノールフタレインのpHと構造変化
以下に示す実験は化学反応により色が変化する実験です。
用意するもの
実験1:振ると青くなる液体
- 水酸化ナトリウム(使用する際は手袋と保護メガネ)
- ブドウ糖 (グルコース)
- メチレンブルー(観賞魚の魚病薬としても売られています)
- 300~500mL のペットボトル
実験2:振ると黄色~赤色~緑色を繰り返す液体(信号反応)
- 水酸化ナトリウム(使用する際は手袋と保護メガネ)
- ブドウ糖 (グルコース)
- インジゴカルミン(合成着色料の一つで食品衛生法では青色2 号として食品添加物に指定されています)
- 300~500mL のペットボトル
実験3:時計反応
- ヨウ素酸カリウム (KIO3)
- 亜硫酸水素ナトリウム (NaHSO3)
- 可溶性デンプン
- チオ硫酸ナトリウム (Na2S2O3)(別名:ハイポと呼ばれペットショップ等で水道などの脱塩素剤として売られている)
- ビーカー
実験手順
実験1 振ると青色になる液
【溶液の調製】
原液
水酸化ナトリウム (NaOH) 2gを水200 mlに溶かす。水酸化ナトリウムは強塩基性で劇物指定です。実験で使うときは手袋、保護メガネ、白衣を着用しましょう。この溶液にブドウ糖 (グルコース:C6H12O6)を 10gを加えて完全に溶かして、300~500mLペットボトルに入れる。この際、ペットボトルの半分から2/3程度にすることが大事です。色素溶液
別の容器にメチレンブルー0.01g(耳かき一杯分位)を20mL の水に溶かす。ペットボトルに入れた①原液に対してメチレンブルー水溶液を少しずつ加える。
【色が変わる実験】
ペットボトルのふたは液が漏れないようにしっかり閉めます。均一になるまで溶液を軽く混ぜて4分程度静置すると無色になります。今度はペットボトルを激しく振ると青色になり、3 分程度静置すると無色に戻ります。この色変化は何回か繰り返すことができます。





【ビデオ:実験1 メチレンブルー】
実験2 軽く振ると黄色から赤色に、強く振ると緑色になる液
【溶液の調製】
原液(実験1と同じです)
水酸化ナトリウム (NaOH) 2gを水200mlに溶かす。水酸化ナトリウムは強塩基性で劇物指定です。実験で使うときは手袋、保護メガネ、白衣を着用しましょう。この溶液にブドウ糖 (グルコース:C6H12O6)を10gを加えて完全に溶かして、300~500mL ペットボトルに入れる。この際、ペットボトルの半分から2/3程度にすることが大事です。色素溶液
別の容器にインジゴカルミン0.1gを10mL の水に溶かす。ペットボトルに入れた①原液に対してインジゴカルミン水溶液を少しずつ加える(およそ0.3~0.6mL)。
【色が変わる実験】
ペットボトルのふたは液が漏れないようにしっかり閉めます。均一になるまで溶液を軽く振って2 分程度静置すると黄色になります。
軽くペットボトルを揺らすと赤色に変化します。さらに激しく振ると緑色になり、1分程度静置すると黄色になります。この色変化は何回か繰り返すことができます。






【ビデオ:実験2 インジゴカルミン】
実験3 時計反応
【溶液の調製】
A液:ヨウ素酸カリウム(KIO3)4.3gを水に溶かして1Lとする
B液:亜硫酸水素ナトリウム水溶液
水 100mL に可溶性デンプン4gを加えて加熱しながら撹拌して、でんぷんが完全に溶けた後に室温まで放冷する。
別の容器に亜硫酸水素ナトリウム(NaHSO3)5.2gを水500mlに溶解する
(1)と(2)を混合し、さらに水を加え1Lとなるようにする。
C 液:チオ硫酸ナトリウム水溶液
チオ硫酸ナトリウム (Na2S2O3) 10g を100mL の水に溶かす。
【色が変わる実験】
① A 液 (150mL)を300mL ビーカーに入れて、B液 (150mL)を加えます。そのまま撹拌しておくと約11秒で急に濃青色に変わります(冬だと約15秒)。




② この色が変わった濃青色溶液にチオ硫酸ナトリウム水溶液(10mL)を加えると無色に変化します。




【ビデオ:実験3 時計反応】
原理
実験1
メチレンブルーは還元状態と酸化状態で構造が異なり、色も還元型では無色、酸化型では青色となります。この還元型から酸化型に変換(酸化)するのは空気中に存在する酸素です。ペットボトルを振ることで上部の空気(酸素)が水溶液に溶け込み、酸化型になります。

図2 メチレンブルーの色変化
また酸化型から還元型への還元反応は塩基性条件でグルコースの還元作用を利用して進行します。その反応は以下の様に示されます。即ち、ブドウ糖(グルコース:C6H12O6) は塩基性(この場合は水酸化ナトリウム)条件下でグルコン酸 (C6H12O7)になり、これが還元剤として働き、ゆっくりと酸化型インジゴカルミンから還元型インジゴカルミンが再生します。

図3 還元剤として作用するグルコース
実験2
インジゴカルミンは塩基性の水溶液では還元型は黄色となりますが、軽く振って少し酸化されると還元型と酸化型の中間構造となり赤色を示します。さらに激しく振ると空気中の酸素によって酸化(空気酸化)され緑色になります。一方、塩基性条件のグルコースは還元作用があり、酸化型インジゴカルミンを徐々に還元型に変化します。

図4 インジゴカルミンの色変化
実験3
ヨウ素でんぷん反応と酸化還元反応を組み合わせた実験です。
① ヨウ素酸カリウム(KIO3)と亜硫酸水素ナトリウム(NaHSO3)が反応すると、式Aが進行し、亜硫酸水素イオン(HSO3-)が反応容器にある限り続きます。しかし亜硫酸水素イオン(HSO3-)が消費されると、式Bの反応が進行しヨウ素(I2)が発生して、ヨウ素デンプン反応により濃青色に変化します。

図5 ヨウ素でんぷん反応を利用した色変化
② ヨウ素デンプン反応により濃青色に変化した溶液にチオ硫酸ナトリウムを加えると、無色になります。これはチオ硫酸ナトリウムによってヨウ素が還元されてヨウ化物イオン (I-)に変化するためです (式C)。レモンや梅干しに含まれるビタミンC (アスコルビン酸) も還元作用があるので同じように色が消えます。水道水には浄水場で殺菌消毒用として少量の塩素(Cl2)を使用され、少量の塩素が水道水に含まれています。金魚などを飼育する水槽の水を交換する際は一日位汲み置きして塩素を除くか、ハイポ(チオ硫酸ナトリウム)を少し入れて塩素を除きます。上記のヨウ素も塩素も同じハロゲン化合物なので、同じ様な反応性が有ります。
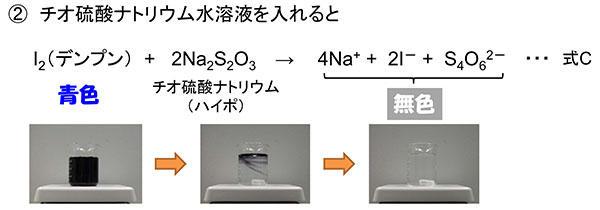
図6 ヨウ素とチオ硫酸ナトリウムの酸化還元を利用した色変化
| 掲載大学 学部 |
山口大学 工学部 | 山口大学 工学部のページへ>> |